Rheumatische Erkrankungen (RA, JIA, PsA): Therapie, Symptome, Ursachen
Die entzündlich-rheumatischen Erkrankungen rheumatoide Arthritis (RA), juvenile idiopathische Arthritis (JIA) und Psoriasis-Arthritis (PsA) unterscheiden sich in Bezug auf Epidemiologie, Symptomatik, Verlauf und Komorbiditäten. Sie weisen jedoch auch Gemeinsamkeiten auf: Sie befallen nicht primär das Achsenskelett, sie treten in Schüben auf, sind mit extraartikulären Manifestationen sowie Komorbiditäten verbunden, können zu schweren Behinderungen führen und beeinträchtigen die Lebensqualität.
Rheumatoide Arthritis
Die rheumatoide Arthritis (RA) ist die häufigste entzündliche Gelenkerkrankung , ihre Prävalenz liegt bei 0,3–1,0 %. Jährlich erkranken in Nordamerika und Europa 20 bis 50 Menschen pro 100.000 Einwohner:innen an einer RA. Frauen sind dreimal so häufig betroffen wie Männer. Der Altersgipfel liegt bei Frauen bei 55 bis 64 Jahren, bei Männern bei 65 bis 75 Jahren.
Unbehandelt führt die Entzündungsaktivität bei rheumatoider Arthritis zur progredienten Gelenkdestruktion mit einem Verlust der Gelenkfunktion und verminderter Lebensqualität. Darüber hinaus wirkt sie sich auch auf die Prognose hinsichtlich von Komorbiditäten und Mortalität aus. Eine frühzeitige krankheitsmodifizierende Behandlung kann die Entzündungsaktivität verringern und die Gelenkzerstörung aufhalten.
Zur medikamentösen Behandlung der rheumatoiden Arthritis stehen symptomatisch wirksame sowie krankheitsmodifizierende Wirkstoffe unterschiedlicher Wirkstoffklassen zur Verfügung. Die nicht medikamentöse Behandlung umfasst eine große Bandbreite physikalischer Therapien und bei Bedarf radiologische Interventionen und chirurgische Eingriffe wie z. B. Synovektomien und Arthrodesen.
ICD-Codes
M05.-, M06.-
Rheumatoide Arthritis: Therapie
Für die Therapieentscheidung, die im Sinne eines „shared decision making“ gleichberechtigt von Patient:in und Ärztin bzw. Arzt getroffen werden sollte, spielen mehreren Faktoren eine Rolle, v. a. jedoch das Ausmaß der Krankheitsaktivität und das Krankheitsstadium.
Das Behandlungsziel bei rheumatoider Arthritis ist die Remission und damit die Verzögerung bzw. Verhinderung der röntgenologisch nachweisbaren Gelenkdestruktion (radiologische Progression). Ein früher Therapiebeginn in den ersten drei bis sechs Monaten nach Symptombeginn führt häufiger zu Remissionen und zum Teil zu einem längeren Remissionserhalt als eine Einleitung der Behandlung in späteren Krankheitsstadien.
Die Patient:innen sollten koordiniert multidisziplinär behandelt werden. Die regelmäßige Dokumentation der Krankheitsaktivität mithilfe validierter Scores wie z. B. dem DAS28 (Disease Activity Score, 28 Gelenke) dient der Qualitätssicherung und Kontrolle des Therapieansprechens und wird im Sinne der Treat-to-target-Strategie zur Anpassung der medikamentösen Behandlung eingesetzt.
Zur medikamentösen Therapie der rheumatoiden Arthritis sind im Einsatz:*,
- Zur Symptomlinderung im Schub oder bis zum Wirkeintritt der krankheitsmodifzierenden Therapie
- Nicht-steroidale Antirheumatika (NSAR), z. B. Diclofenac, Ibuprofen, Naproxen, Indometacin
- Glukokortikoide, z. B. Prednisolon
- Opioide
- Basistherapeutika oder krankheitsmodifizierende Medikamente (disease modifying antirheumatic drugs, DMARDs)
- Konventionelle synthetische DMARDs (csDMARDs), z. B. Methotrexat, Leflunomid, Sulfasalazin, Hydroxychloroquin
- Biologische DMARDs (Biologika), z. B. TNF-α-Hemmer wie Adalimumab, Etanercept, Infliximab, Certolizumab, Golimumab; T-Zell-Aktivierungshemmer wie Abatacept; Interleukin-6-Rezeptor-Antikörper wie Tocilizumab, Sarilumab; B-Zell-Antikörper wie Rituximab; Interleukin-1-Konkurrenten wie Anakinra
- Zielgerichtete synthetische DMARDs (ts(targeted synthetic)DMARDs), z. B. JAK-Inhibitoren wie Baricitinib, Tofacitinib
*Für genauere Informationen siehe entsprechende Fachinformationen
Darüber hinaus werden je nach Bedarf invasive (chirurgische und radiologische), physikalische und supportive Behandlungsverfahren eingesetzt:
- Invasive Therapie: Gelenkpunktion, intraartikuläre Injektionen, Radiosynoviorthese, Synovektomie, Gelenkersatz
- Zusätzliche Therapien: Physiotherapie (Manuelle Therapie, Thermo- und Elektrotherapie), Ergotherapie, Rehabilitation, Bewegungstherapie, Entspannungstechniken, psychologische Unterstützung
Rheumatoide Arthritis: Symptome und Folgen
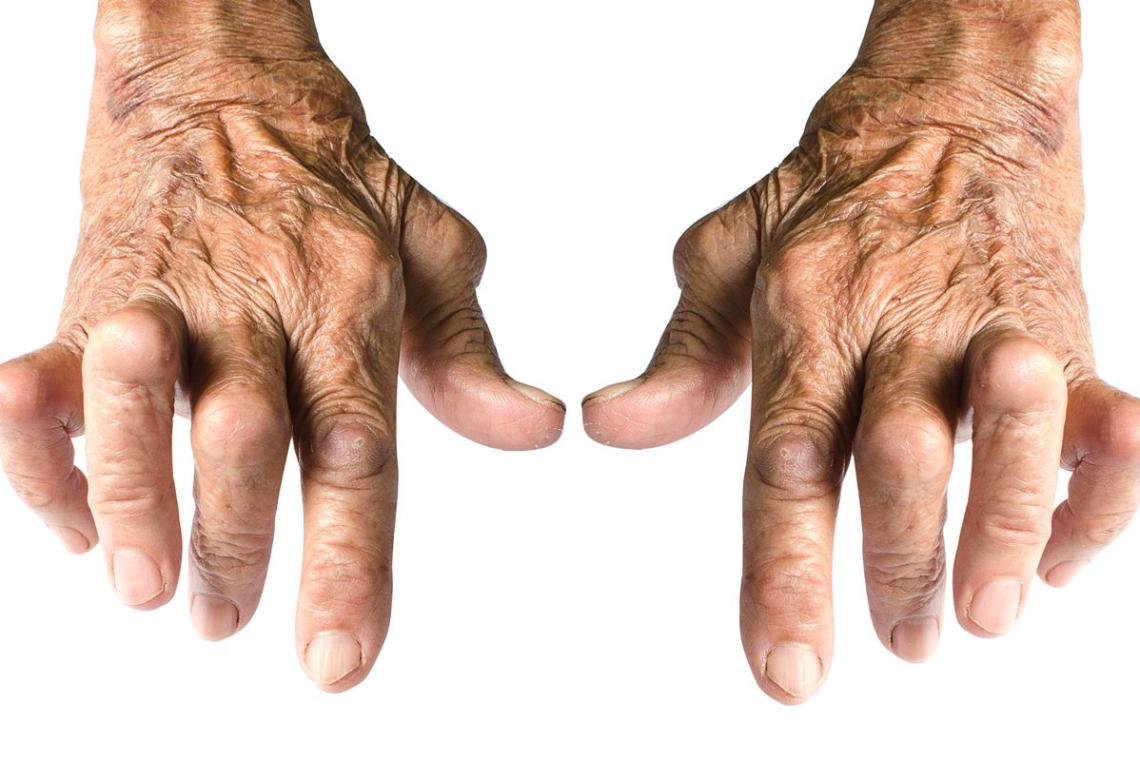
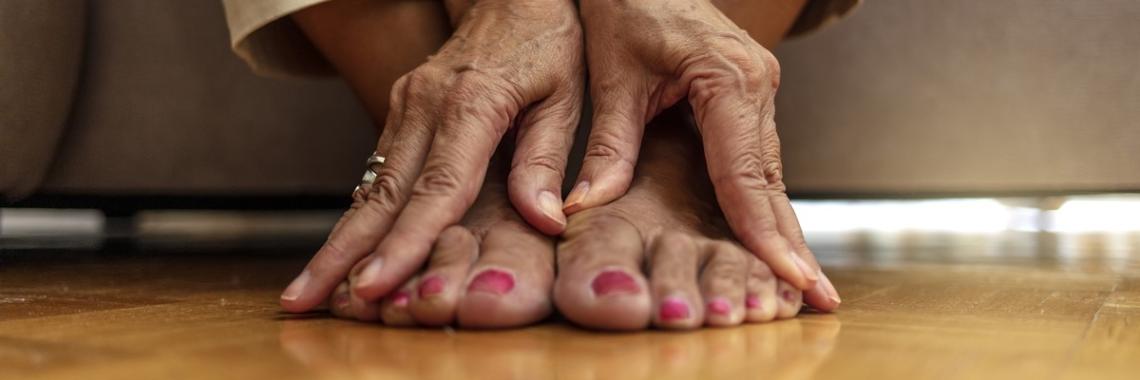
Anfangs treten häufig grippeähnliche Allgemeinsymptome auf, etwa Müdigkeit, Abgeschlagenheit, leichtes Fieber, Schweregefühl der Muskeln und Appetitlosigkeit. Im Verlauf kommt es zu schmerzhaften, weichen, teigigen Gelenkschwellungen. Am häufigsten davon betroffen sind Hand-, Fingergrund(MCP)- und Fingermittel(PIP)-Gelenke, daneben auch Zehengrund (MTP)-, Ellenbogen-, Schulter-, Knie- und Sprunggelenke.Der Befall des Atlantoaxialgelenks kann zur zervikalen Instabilität führen, die als gefürchtete Komplikation der RA gilt.
Bei der extraartikulären Manifestationen (EAM) der rheumatoiden Arthritis sind neben den Gelenken weitere Strukturen und Organe befallen (siehe Tabelle 1).
Tabelle 1: Extraartikuläre Manifestationen der rheumatoiden Arthritis
| Nicht schwere EAM | |||||||||
|---|---|---|---|---|---|---|---|---|---|
|
|||||||||
| Schwere EAM | |||||||||
|
Rheumatoide Arthritis: Diagnose
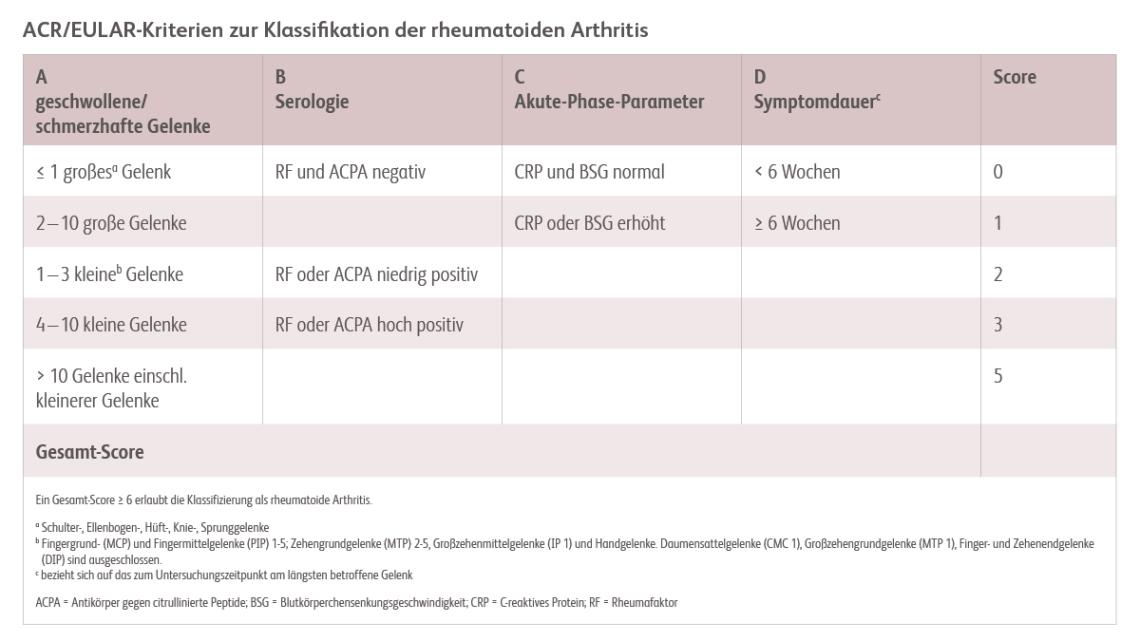
Die Diagnose der frühen rheumatoiden Arthritis kann sich schwierig gestalten. Die ACR/EULAR-Klassifikationskriterien erleichtern die Diagnosestellung. Sie berücksichtigen den Gelenkbefall, Serostatus, Akute-Phase-Parameter (C-reaktives Protein und Blutkörperchen-Senkungsgeschwindigkeit) sowie die Symptomdauer (siehe Abbildung).
Tabelle 2: Klinische Stadien der rheumatoiden Arthritis
|
Stadium I: Frühstadium
|
|
Stadium II: mäßig fortgeschritten
|
|
Stadium III: weit fortgeschritten
|
|
Stadium IV: Endstadium
|
Rheumatoide Arthritis: Ursachen
Die Ursache der Autoimmunerkrankung rheumatoide Arthritis ist noch nicht zur Gänze geklärt. Es werden jedoch genetische Faktoren und Umweltfaktoren als Auslöser der RA angenommen.
- Zu den genetischen Faktoren zählen u. a. die MHC-Gene (MHC = major histocompatibility complex), die humane Leukozytenantigene (HLA) kodieren, welche für die Unterscheidung „selbst“ und „fremd“ zuständig sind. Es gibt Hinweise darauf, dass das HLA-DR-assoziierte RA-Risiko im Zusammenhang mit einer erhöhten Antigenpräsentation veränderter Proteine durch HLA-Moleküle basiert. HLA-DR ist ein MHC-Klasse-II-Rezeptor auf der Oberfläche von antigenpräsentierenden Immunzellen, der mit Fremdeiweiß einen Komplex bildet, der die Immunantwort der T-zellen stimuliert.
- Als einer der wichtigsten Umweltfaktoren gilt das Rauchen. Daneben werden Infektionen mit dem Epstein-Barr-Virus (EBV) sowie verschiedenen Bakterien als Auslöser einer Autoimmunität genannt. Auch Allergien werden als mögliche Ursachen diskutiert.
Pathogenese der rheumatoiden Arthritis
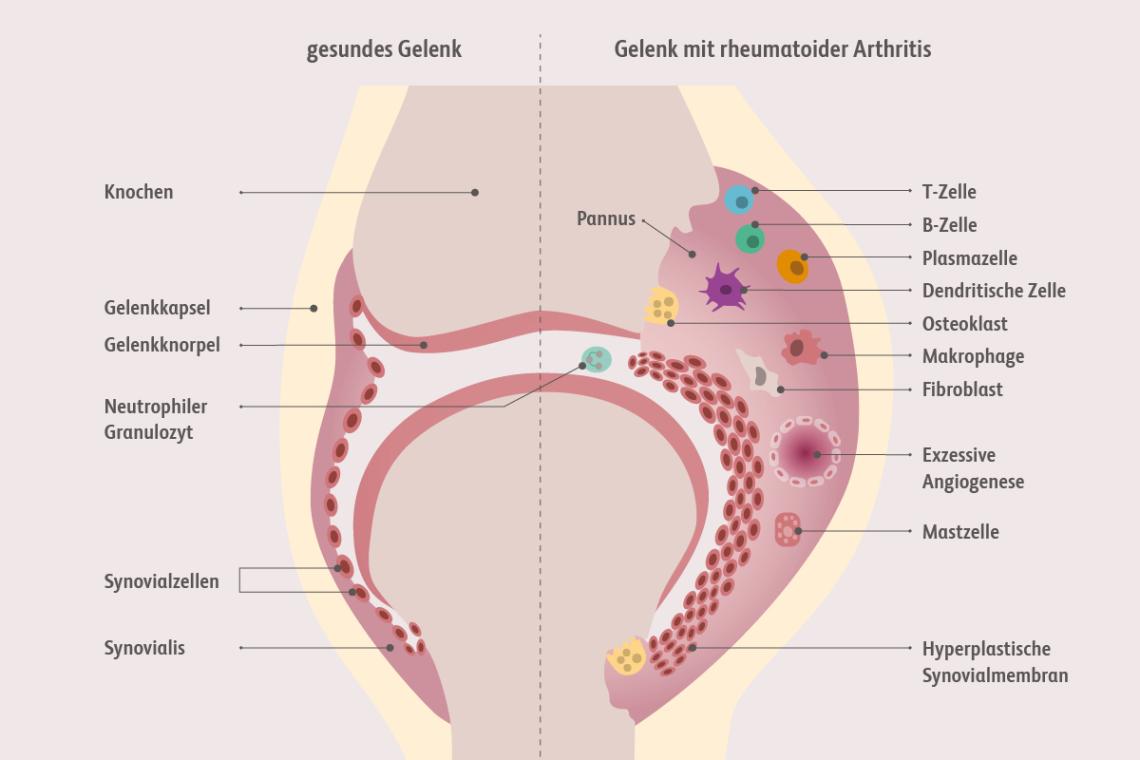
Durch ein komplexes Zusammenspiel genetischer Faktoren und Umweltfaktoren kommt es zu einer gestörten Immuntoleranz, zur Produktion von Autoantikörpern und einer durch Freisetzung pro-entzündlicher Zytokine (z. B. TNF, Interleukine) bedingten und unterhaltenen Entzündung der Synovialmembran.
Durch Gefäßneubildung und Einwanderung von verschiedenen mononukleären Zellen kommt es in der Synovialmembran zur Entstehung eines Pannus, der den Gelenkknorpel angreift und letztlich zerstört. Dazu kommt die durch Osteoklastenaktivierung bedingte typische Destruktion des Knochens.
Juvenile idiopathische Arthritis
Die juvenile idiopathische Arthritis (JIA) ist eine autoimmun-bedingte entzündliche Erkrankung im Kindes- und Jugendalter, deren Ätiologie noch nicht zur Gänze geklärt ist. Zur Krankheitsentstehung scheinen genetische Faktoren und Umweltfaktoren beizutragen. Die juvenile idiopathische Arthritis betrifft Kinder jeglichen Alters sowie Jugendliche und ist mit einer Prävalenz von ca. 0,1 % die häufigste entzündlich-rheumatische Erkrankung in dieser Altersgruppe.
Die JIA ist definiert als eine Arthritis unklarer Ursache von mindestens sechs Wochen Dauer, die vor dem vollendeten 16. Lebensjahr beginnt. Sie wird nach ihrem klinischen Erscheinungsbild in sechs definierte Subtypen und eine nicht definierte Gruppe („andere Arthritis“) eingeteilt.
Die juvenile idiopathische Arthritis ist eine chronische Erkrankung, die schwere klinischen Symptome und extraartikuläre Manifestationen (EAM), v. a. eine Uveitis, aber auch Erkrankungen des Herzens, der Nieren, der Haut und der lymphatischen Organe verursachen kann. Sie ist mit einem erhöhten Risiko für Morbidität verbunden, u. a. Gelenkzerstörung, Osteoporose und Beeinträchtigung der Sehkraft infolge der Uveitis. Es besteht auch das Risiko einer verkürzten Lebenserwartung und einer Entwicklungsbeeinträchtigung. Psychische Komorbiditäten sind nicht selten und es drohen Behinderung mit verminderter Lebensqualität sowie eingeschränkter Teilhabe am täglichen Leben.
Zur Behandlung der JIA werden, wie bei der rheumatoiden Arthritis, symptomatisch wirksame und krankheitsmodifizerende Wirkstoffe eingesetzt.
ICD-Code
M08.-
Juvenile idiopathische Arthritis: Therapie
Die Therapie der juvenilen idiopathischen Arthritis sollte möglichst früh beginnen. Ziel ist die rasche und wirksame Kontrolle der Entzündungsaktivität mit der Induktion einer Remission und deren Erhalt. Des Weiteren sollten krankheits- und/oder therapiebedingte Folgeschäden vermieden sowie die somatische und psychosoziale Entwicklung, optimale Alltagsfunktion, Lebensqualität und Teilhabe der kindlichen/jugendlichen Patient:innensichergestellt werden.
Die Behandlung orientiert sich an den Subtypen, sollte aber auch Krankheitsaktivität, extraartikuläre Manifestationen, Verlauf, Funktionsdefizite sowie Alter und Entwicklungsstand der Patient:innen berücksichtigen. Dazu ist die Versorgung durch Kinder-/Jugendrheumatolog:innen und speziell geschulte Fachkräfte erforderlich.
Für die Therapie der juvenilen idiopathischen Arthritis werden eingesetzt:*,
- Glukokortikoide, z. B. Prednisolon
- Nicht-steroidale Antirheumatika, z. B. Diclofenac, Ibuprofen, Naproxen, Indometacin
- Basistherapeutika oder krankheitsmodifizierende Medikamente (disease modifying antirheumatic drugs, DMARDs)
- Konventionelle synthetische DMARDs (csDMARDs), z. B. Methotrexat, Sulfasalazin, Leflunomid
- Biologische DMARDs (bDMARDs, Biologika), z. B. TNF-α-Hemmer wie Adalimumab, Etanercept, Golimumab; T-Zell-Aktivierungshemmer wie Abatacept; Interleukin-6-Rezeptor-Antikörper wie Tocilizumab; Interleukin-1-Konkurrenten wie Anakinra, monoklonale Interleukin-1β Antikörper wie Canakinumab
*Für genauere Informationen siehe entsprechende Fachinformationen
- Zusätzliche Therapien: Physiotherapie, Ergotherapie, psychosoziale Unterstützung etc.
Formen der juvenilen idiopathischen Arthritis
Die juvenile idiopathische Arthritis ist eine heterogene Gruppe von Krankheiten. Sie umfasst sechs definierte Kategorien der JIA und eine nicht definierte Gruppe („andere Arthritis“). Die Kategorisierung der JIA erfolgt nach den ILAR-Kriterien, sie fußt auf klinischen Parametern (z. B. der Zahl der in den ersten sechs Erkrankungsmonaten betroffenen Gelenke), extraartikulären Manifestationen, wenigen Laborparametern sowie der Familienanamnese.
Systemische juvenile idiopathische Arthritis (sJIA)
- Arthritis und Fieber (intermittierend, Dauer mindestens zwei Wochen) und mindestens ein weiteres Kriterium: flüchtiger erythematöser Hautausschlag, generalisierte Lymphadenopathie, Hepato- und/oder Splenomegalie, Serositis
- Allgemeinsymptome können der (Poly)Arthritis um Monate vorangehen
- Hohe Entzündungsaktivität kann auch heute noch zu Kleinwuchs und Amyloidose führen
Oligoartikuläre juvenile idiopathische Arthritis (oJIA)/Oligoarthritis (OA)
- Arthritis von maximal vier Gelenken innerhalb der ersten sechs Erkrankungsmonate, oft Knie-, Sprung- oder Handgelenke, Allgemeinsymptome fehlen, erhöhtes Risiko für eine Uveitis
- Häufigste Form der JIA, Erkrankungsbeginn meist im Vorschulalter, Mädchen sind häufiger betroffen
Polyartikuläre juvenile idiopathische Arthritis (pJIA)/Polyarthritis, seropositive und seronegative Form
- Arthritis in > vier Gelenken, während der ersten sechs Erkrankungsmonate , häufig symmetrisch , Beteiligung der Kiefergelenke und der Halswirbelsäule möglich
- Seronegative (häufiger) oder seropositive Subgruppe
Juvenile Psoriasis-Arthritis
- Arthritis und Psoriasis oder Arthritis und mindestens zwei der folgenden Kriterien: Daktylitis; Nagelveränderungen (Tüpfelung oder Onycholyse); Psoriasis bei einem Verwandten ersten Grades
- Kann mit Augenbeteiligung, Polyarthritis oder wie eine Arthritis mit Enthesitisneigung verlaufen
Enthesitis-assoziierte JIA
- Arthritis und Enthesitis oder Arthritis und mindestens zwei der folgenden Kriterien: Druckschmerz über den Iliosakralgelenken und/oder entzündlicher Rückenschmerz lumbosakral, akute (symptomatische) anteriore Uveitis
- Jungen mit HLA-B27-Nachweis häufiger betroffen
- Erkrankungsbeginn > sechs Jahre
- Enthesitis-assoziierte Arthritis, ankylosierende Spondylitis, Sakroiliitis bei entzündlicher Darmerkrankung, Reiter-Syndrom oder akute anteriore Uveitis bei einem Angehörigen ersten Grades
- Häufig Übergang in eine Spondylarthropathie
Andere Arthritis
Psoriasis-Arthritis
Die Psoriasis-Arthritis (PsA, psoriatische Arthritis) ist eine chronisch verlaufende Autoimmunerkrankung der Gelenke. Ihr Erscheinungsbild bei Patient:innen mit bestehender oder latenter Psoriasis ist heterogen. Die Ursache der Psoriasis-Arthritis ist noch nicht abschließend geklärt, vermutlich basiert sie auf dem Zusammenwirken von genetischen Faktoren und Umweltfaktoren. Die Gelenkentzündung kann unbehandelt zu schweren Schädigungen mit Deformationen und Funktionseinbußen führen.
Die Prävalenz der PSA liegt bei ca. 30 % der Psoriasis-Patient:innen, wobei die psoriatische Hauterkrankung in etwa 80 % der Fälle vor den Gelenksymptomen besteht. In seltenen Fällen beginnt die Psoriasis-Arthritis mit oder sogar vor den ersten Hautsymptomen. Der Erkrankungsgipfel liegt zwischen 35 und 55 Jahren.
Mögliche extraartikuläre Manifestationen schließen eine chronisch-entzündliche Darmerkrankung sowie eine Uveitis mit ein. Darüber hinaus ist die Psoriasis-Arthritis mit einer Reihe von Komorbiditäten assoziiert, u. a. kardiovaskulären, psychologischen und Stoffwechselerkrankungen. Insgesamt ist die Krankheitslast durch die PsA erheblich, die Lebensqualität beeinträchtigt und die Lebenserwartung verringert.
ICD-Codes
M07.-, M09.-
Psoriasis-Arthritis: Behandlung
Wie bei anderen entzündlich-rheumatischen Erkrankungen sollte auch bei der Psoriasis-Arthritis die interdisziplinäre Behandlung frühzeitig begonnen werden, um eine Gelenkdestruktion zu verhindern. Das Behandlungsziel ist die Remission oder zumindest eine niedrige Krankheitsaktivität. Mithilfe validierter Instrumente sollte das Erreichen des Behandlungsziels regelmäßig überprüft und bei ungenügendem Ansprechen die Therapie angepasst werden (treat to target).
Die Therapieentscheidung orientiert sich gemäß den GRAPPA-Empfehlungen an den Krankheitsmanifestationen (periphere Arthritis, axiale Arthritis, Daktylitis, gleichzeitiger Haut-und/oder Nagelbefall).
Eingesetzt werden zur Psoriasis-Arthritis-Therapie:*,
- Glukokortikoide, z. B. Prednison
- Nicht-steroidale Antirheumatika/NSRA, z. B. Diclofenac, Ibuprofen, Indometacin
- Basistherapeutika ("disease modifying antirheumatic drugs", DMARDs)
- Konventionelle synthetische DMARDs (csDMARDs), z. B. Methotrexat, Leflunomid, Sulfasalazin, Ciclosporin A
- Biologische DMARDs (Biologika), z. B. TNF-α-Antagonisten wie Etanercept, Infliximab, Adalimumab, Golimumab, Certolizumab; T-Zell-Aktivierungshemmer wie Abatacept; IL-12/23-Inhibitoren wie Ustekinumab; IL-17A-Inhibitoren wie Secukinumab
- Zielgerichtete synthetische DMARDs (tsDMARDs), z. B. JAK-Inhibitoren
*Für genauere Informationen siehe entsprechende Fachinformationen
- Zusätzliche Therapien: Physiotherapie, Ergotherapie, topische Therapien bei Haut- und Nagelbeteiligung, psychosoziale Interventionen
Informationen zur Therapie der Psoriasis-Arthritis von Bristol Myers Squibb finden Sie hier.
Psoriasis-Arthritis: Symptome
Hauptsymptom der Psoriasis-Arthritis ist eine schmerzhafte Oligo- oder Polyarthritis. Im Gegensatz zur rheumatoiden Arthritis, sind bei der PsA typischerweise die Finger- und Zehenendgelenke (DIP) betroffen. Auch der Befall des gesamten Strahls ist möglich. Dazu kommen Morgensteifigkeit, nächtliche Schmerzen sowie Funktionseinschränkungen. Bei axialem Befall tritt häufig eine Sakroiliitis mit positivem HLA-B27-Nachweis auf. Enthesitis, Daktylitis (Wurstfinger, Wurstzehen) sowie für Psoriasis typische Haut- und Nagelveränderungen werden ebenfalls beobachtet , wobei die Daktylitis praktisch beweisend für die PsA ist.